Αναζήτηση
ΚΛΕΙΣΙΜΟΆμεση Απόδειξη Αποϋδάτωσης Πρωτεϊνών σε Όξινες Συνθήκες
Direct evidence of acid-driven protein desolvation
F. Hamdi, I. Skalidis, I.K. Schwerin, J. Belapure, D.A. Semchonok, F.L. Kyrilis, C. Tüting, J. Müller, G. Künze, & P.L. Kastritis
Proceedings of the National Academy of Sciences (PNAS), 2026, 123 (10) e2525949123
Ένα νέο ερευνητικό άρθρο, στο οποίο συνυπέγραψαν ο καθηγητής Παναγιώτης Καστρίτης (συγγραφέας αλληλογραφίας) και ο Δρ. Φώτης Κυρίλης, δημοσιεύθηκε σε ένα από τα πιο έγκριτα επιστημονικά περιοδικά διεπιστημονικού χαρακτήρα: το Proceedings of the National Academy of Sciences (PNAS).
Η μελέτη με τίτλο “Direct evidence of acid–driven protein desolvation“ (Hamdi et al., 2026) διερευνά ένα μακροχρόνιο ερώτημα της βιοχημείας σχετικά με τη συμπεριφορά των μορίων νερού γύρω από τις πρωτεΐνες σε όξινες συνθήκες. Μέσω απεικόνισης σε ατομικό επίπεδο, παρατηρήθηκε ότι με την αύξηση της οξύτητας απομακρύνονται εκατοντάδες μόρια νερού, ενώ ένα οργανωμένο κέλυφος ενυδάτωσης παραμένει εν μέρει διατηρημένο.
Τα αποτελέσματα δείχνουν επίσης ότι η οξύτητα επηρεάζει τη δέσμευση μετάλλων, όπως ο σίδηρος, στις πρωτεΐνες, προσφέροντας νέες γνώσεις για τους μηχανισμούς ενυδάτωσης και τη σταθερότητα των πρωτεϊνών.
Direct evidence of acid-driven protein desolvation
F. Hamdi, I. Skalidis, I.K. Schwerin, J. Belapure, D.A. Semchonok, F.L. Kyrilis, C. Tüting, J. Müller, G. Künze, & P.L. Kastritis
Proceedings of the National Academy of Sciences (PNAS), 2026, 123 (10) e2525949123
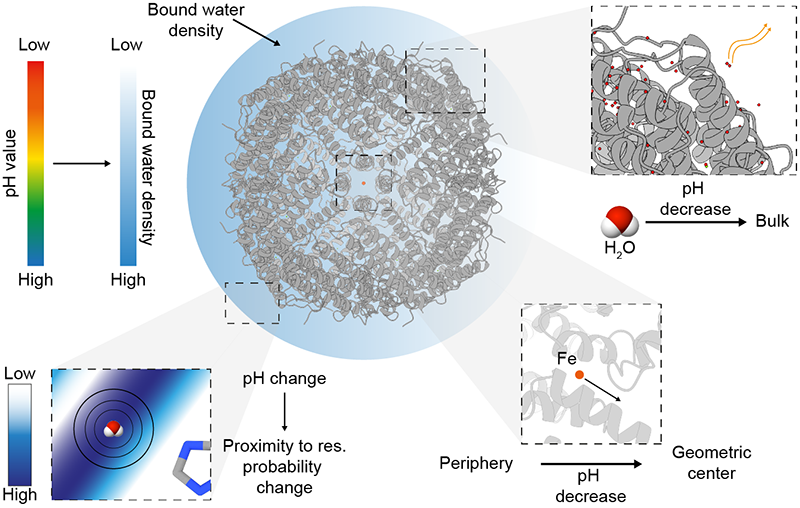
Κεντρική εικόνα σελίδας: Solvation layer effects as a function of pH. The modeled waters belonging to the solvation layer numerically differ with decreasing pH. The density of bound waters decreases with decreasing pH, moving toward the bulk and not contributing to protein complex stabilization, whereas the probability distribution of water-molecule localization in proximity to the nearest amino acid side chain becomes narrower. Fe atoms are affected by water density, being pushed to the geometric center of the protein complex
